| kategória | ||||||||||
|
|
||||||||||
|
|
||
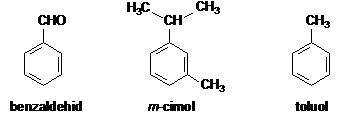
A telítetlen gyürüs szénvegyületek körében különleges szerkezetük miatt az aromás szénhidrogének sajátos csoportot képviselnek. Az aromás elnevezés régi keletü és utal e vegyületek illatára (aromájára), mivel számos képviselöjüket kellemes illatú növényi anyagokból (gyantákból, balzsamokból, illóolajokból stb.) izolálták. Például, a keserümandula olajából benzaldehid, a köményolajból meta-cimol különíthetö el, a tolubalzsam hevítése során pedig toluol képzödik.
Az aromás vegyületek - szerkezetüket tekintve - mind a C6H6 összegképletü ben 646b15g zolból származtathatók, többségük a benzol helyettesített származéka. A benzol már 1825 óta ismert vegyület. Faraday az olajgáz komprimálása során fedezte fel. Néhány évvel késöbb Mitscherlich (1833) a benzoegyantából nyert benzoesav kálciumsójának hevítésével is elöállította és "benzin"-nek nevezte el. Mivel az in végzödésü nevekkel akkoriban az alkaloidokat (pl. morfint) jelölték, Faraday a benzol nevet javasolta. Ezt a nevet vette át Hofmann (1845) is, aki elöször különítette el a köszénkátrányból a benzolt tiszta és egységes állapotban. Ugyancsak Hofmann úttörö vizsgálatai nyomán vált ismertté, hogy a köszénkátrány aromás vegyületekben igen gazdag. A köszén szervesanyag-állománya magas hömérsékletre (900-1300 C) melegítve mélyreható változást szenved, belöle ún. száraz lepárlással gáz, folyadék és szilárd halmazállapotú termékek különíthetök el. Gáz-halmazállapotú a világítógáz (kokszgáz). A hütésre kondenzálódó termék vizes fázisra (gázvírezre) és egy vízzel nem elegyedö részre (kátrányra) különül el. A lepárlóban visszamaradó szilárd anyag a koksz. E termékek közül a világítógáz is számottevö mennyiségü benzolt és naftalint tartalmaz, de az aromás szénhidrogének nagyobb mennyiségben a köszénkátrány további frakcionált desztillációjával nyerhetök. Jóllehet a történeti eredetü aromás elnevezést ma is használjuk, de ma már e név nem a vegyületek illatára, aromájára utal, hanem szerkezetük jellegére. Ugyanis az olyan gyürüs telítetlen vegyületeket, melyek különleges szerkezetük miatt rendkívül stabilak, oxidációs és addíciós reakcióra nem hajlamosak, viszont könnyen vihetök típustartó elektrofil szubsztitúciós (SEAr) reakciókba, aromás vegyületeknek nevezzük.
Az aromás szénhidrogéneket szerkezetük alapján az alábbiak szerint csoportosítjuk.
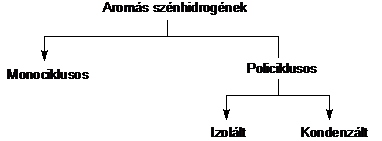
A monociklusos aromás szénhidrogének molekuláikban csupán egyetlen aromás gyürüt tartalmaznak. Gyakorlati szempontból közülük a legfontosabbak a már említett benzol és származékai.
Az aromás szénhidrogének - általános nevükön arének - monociklusos származékait általában a benzol szubsztituált származékaiként nevezzük el, azonban néhány rövidebb alifás oldalláncot tartalmazó szénhidrogénnek triviális neve is van.
|
Szerkezet |
Triviális név |
Szubsztitúciós név |
|
|
benzol |
|
|
|
toluol |
metilbenzol |
|
|
o-, m-, p-xilol |
o-, m-, p-dimetilbenzol |
|
|
mezitilén |
1,3,5-trimetilbenzol |
|
|
kumol |
izopropilbenzol |
|
|
sztirol |
vinilbenzol |
A xilol is példázza, hogy a diszubsztituált származékok esetén szerkezeti izoméria lép fel. A gyürü számozása az aliciklusos szénhidrogéneknél már megismert módon (l. ???. old.) történik. Ha a triviális névvel rendelkezö szénhidrogént tekintjük alapvegyületnek, akkor a legkisebb számot az alapvegyületen már jelenlévö szubsztituens kapja. Diszubsztituált származékoknál az 1,2-, 1,3- és 1,4-számozás helyett az o- (orto), m- (meta) és a p- (para), jelölés is használható.
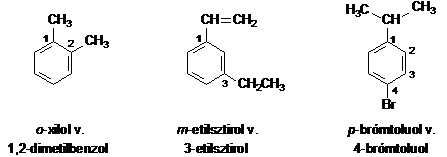
Két azonos vagy különbözö szubsztituens esetén három (o-, m-, p-), három azonos szubsztituens esetében ugyancsak három (1,2,3-; 1,2,4-; 1,3,5-), két azonos, valamint egy eltérö szubsztituens esetén hat, és három különbözö szubsztituens esetén pedig tíz szerkezeti izomer lehetséges.
Az arénekböl (ArH) levezethetö egyvegyértékü csoportot általánosan arilcsoportnak (Ar-) nevezzük, azonban benzol vagy toluol esetén fenilcsoportról (Ph-), illetve o-, m- vagy p-tolilcsoportról beszélünk.
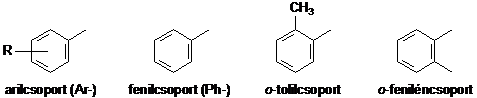
Ugyancsak a benzolból vezethetö le a két szabadvegyértékü o-, m- és p-feniléncsoport.
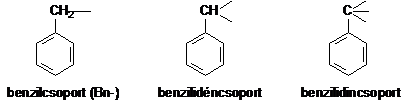
A benzolgyürühöz kapcsolódó alkilcsoportokat szokás oldalláncnak, magát a gyürüt pedig aromás magnak is nevezni. A legrövidebb oldallánc a metilcsoport, melyböl a benzil- (Bn-), a benzilidén- és a benzilidincsoport származtatható a megfelelö számú hidrogén elvételével.
A legegyszerübb és a legfontosabb monociklusos aromás szénhidrogén a benzol, melynek szerkezetét az elemi összetétel (C:H = 1:1) alapján 1865-ben Kekulé az alábbi módon tüntette fel.
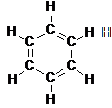
Kekulé feltételezte, hogy a gyürüt alkotó szénatomok egyszeres és kétszeres kötésekkel kapcsolódnak egymáshoz. Elképzeléseit sokan (pl. Baeyer, Claus, Ladenburg, Thiele) bírálták, azzal érvelve, hogy a benzolnak "háromszoros" telítetlensége miatt oxidatív behatásokkal (pl. Baeyer-reakcióval) szemben sokkal érzékenyebbnek kellene lennie, mint az eténnek, és a halogénekkel vagy hidrogénnel is készségesen kellene reagálnia. Ezzel szemben azt tapasztalták, hogy a benzol nagyon stabil vegyület. A Baeyer-reakciót nem adja, és mind a hidrogén, mind pedig a halogének csak nehezen addícionálhatók benzolra. Ladenburg kritikáját, miszerint a benzolnak a kísérleti tapasztalattal ellentétben voltaképpen két különbözö 1,2- diszubsztituált származéka léteznék aszerint, hogy a két szubsztituenst a gyürüben egyszeres (A) vagy kétszeres (B) kötés választja el, Kekulé az ún. áramló kötések elvének bevezetésével hárította el.

A mechanikai
höelmélet alapján feltételezte, hogy a szénatomok hörezgése miatt a
kettös kötések nem rögzítettek és szüntelenül változtatják a helyzetüket (A![]() B). Jóllehet ezzel az elképzeléssel a
benzol addíciós és oxidációs reakciókban mutatott csekély reaktivitását
megmagyarázni nem lehetett, de a kettös kötések folytonos "vándorlását"
illetöen Kekulé megállapítása
lényegében helytállónak bizonyult. A benzol elektronszerkezetének különféle
spektroszkópiai módszerekkel (UV, IR, NMR és röntgendiffrakció) igazolt pontos
magyarázata Hückel nevéhez
füzödik. Értelmezése szerint a molekulapálya
elmélet (MO) alapján a benzol három elektronállapota a következö:
B). Jóllehet ezzel az elképzeléssel a
benzol addíciós és oxidációs reakciókban mutatott csekély reaktivitását
megmagyarázni nem lehetett, de a kettös kötések folytonos "vándorlását"
illetöen Kekulé megállapítása
lényegében helytállónak bizonyult. A benzol elektronszerkezetének különféle
spektroszkópiai módszerekkel (UV, IR, NMR és röntgendiffrakció) igazolt pontos
magyarázata Hückel nevéhez
füzödik. Értelmezése szerint a molekulapálya
elmélet (MO) alapján a benzol három elektronállapota a következö:
egyetlen atommag eröterében mozgó elektronok. Ilyenek a szénatom lezárt 1s pályáján lévö elektronpárok;
elektronpáronként két-két atommag közös eröterében mozgó elektronok, melyek a szén-szén és a szén-hidrogén közötti s kötéseket alakítják ki;
az sp2-hibridállapotú szénatomok 2pz pályáin lévö elektronok, melyek eloszlása - mint azt az alkének szerkezetének tárgyalásakor már bemutattuk (l. ???. old.) - a s-váz síkjának két oldalán koncentrálódik és ezek alkotják a molekula p-elektronrendszerét.
Ennek megfelelöen a Hückel-féle molekulapálya-módszer (rövidítve HMO-módszer) szerint a benzolmolekulában elkülönül a s-váz és a p-elektronrendszer. Az utóbbi a szénatomok 2pz pályáinak kölcsönhatásából (matematikailag lineáris kombinációként) alakul ki, és a hat atompálya (pz) kombinációjával hat molekulapálya képzödik.
Mint már kifejtettük (l. ???. old.) az elmélet alapja: a szimmetriafeltételek által megengedett maximális számú atompálya azonos elöjellel történö kombinációja. Az atompályák azonos elöjelü ún. kötö jellegü kombinációja energetikailag kedvezöbb, mint az ellentétes elöjelü pályáké, amelyek lazító jellegüek. A molekulapálya energiája a csomósíkok számának növekedésével nö. Az így kialakuló molekulapályák szimmetriája megfelel a molekula szimmetriaviszonyainak, vagyis a benzol szimmetriaelemeire vonatkoztatva minden molekulapálya szimmetrikus vagy antiszimmetrikus. A benzol molekulapályáit és energiadiagramját a 2.7. ábrán tüntettük fel úgy, hogy a pz-pályáknak csak a gyürü egyik térfelére esö részletét ábrázoltuk. A sötét és világos körökkel jelöltük a kölcsönhatásban lévö atompályák fázisát, a körök nagyságával pedig az egyes atompályák hozzájárulásának (ci) mértékét érzékeltettük.
A benzolmolekula hat szénatomjához tartozó hat pz-pálya legkedvezöbb, azaz legkisebb energiaértékü kombinációja (p ) úgy valósul meg, hogy a pz-pályák azonos fázisban lépnek kölcsönhatásba egymással, és így az elektronsürüség minden szénatom felett és alatt azonos.
Találat: 3244