| kategória | ||||||||||
|
|
||||||||||
|
|
||
KOMPLEX VEGYÜLETEK
Vizes oldatokban a fémionok a vízmolekulákkal koordinált kovalens kötéseket létesítenek. A periódusos rendszer s-mezöjében található fémionok (kis töltésü és nagy átméröjü ionok) lazán kötött hidrátokat képeznek. A kis átméröjü és nagy töltésü ionok (mint amilyenek a d-mezö fémionjai) erösen kötött, stabil hidrátokat hoznak létre a vízzel. A kialakuló kötést a Lewis-féle elmélettel értelmezhetjük, ugyanis a fémion a Lewis-féle savnak (elektronpár akceptor), 616i88g az elektronpár donor H2O molekula pedig Lewis-bázisnak tekinthetö. Az ilyen vagy hasonló módon kialakuló összetett ionokat vagy molekulákat komplexeknek nevezzük. (Fématomok vagy fémionok kapcsolódnak semleges molekulákhoz vagy anionokhoz datív kötéssel). Jelen esetben, mivel vízmolekulák vesznek részt elektronpár donorként a komlexképzödésben, akvakomplexekröl beszélünk. A Cu2+ vagy Ag+ vizes oldatában az alábbi hidratált ionformák (akvakomplexek) alakulnak ki:
![]() Cu2+
+ H2O(l) [Cu(H2O)]2+
Cu2+
+ H2O(l) [Cu(H2O)]2+
.
.
.
.
![]() [Cu(H2O)5]2+
+ H2O(l) [Cu(H2O)6]2+
[Cu(H2O)5]2+
+ H2O(l) [Cu(H2O)6]2+
![]() Ag+
+ 2 H2O(l) [Ag(H2O)2]+
Ag+
+ 2 H2O(l) [Ag(H2O)2]+
A koordinált kötésü vízmolekulákat vizes oldatban részben vagy teljesen helyettesíthetik olyan molekulák vagy ionok, amelyek Lewis-bázisként viselkedve elektronpár átadására alkalmasak. Például ammóniamolekulával a vízmolekulákat helyettesítve az alábbi komplexet kapjuk:
![]() [Ag(H2O)2]+
+ 2 NH3(aq) [Ag(NH3)2]+
+ 2 H2O(l)
[Ag(H2O)2]+
+ 2 NH3(aq) [Ag(NH3)2]+
+ 2 H2O(l)
amelyben a nitrogénion az elektronpár donor.
A hat vízmolekulát tartalmazó [hexaakva-ferrát(II)] ionban a vízmolekulák egymás után kicserélhetök cianidionokkal:
![]() [Fe(H2O)6]2+
+ CN (aq) [FeCN(H2O)5]+
+ H2O(l),
[Fe(H2O)6]2+
+ CN (aq) [FeCN(H2O)5]+
+ H2O(l),
.
.
.
.
Utolsó lépcsöként az alábbi folyamat megy végbe:
![]() [Fe(CN)5(H2O)]3-
+ CN (aq) [Fe(CN)6]4 + H2O(l).
[Fe(CN)5(H2O)]3-
+ CN (aq) [Fe(CN)6]4 + H2O(l).
Ennek eredményeként végül is a vas(II)ion hat cianidionnal alkot datív (koordinált kovalens) kötést.
A fémkomplexek szerkezete
Az elözöekböl kiderült, hogy a fémkomplexek képzödésében a fémen kívül elektrondonorként funkcionáló semleges molekulák vagy anionok vesznek részt. A kialakuló struktúrában a fémet központi atomnak, az említett kapcsolódó részeket pedig ligandumoknak nevezzük. Aszerint hogy ezek hány szabad elektronpárral rendelkeznek, egy, két ill. többfunkciós ligandumokról beszélünk. (Más elnevezéssel egyfogú, kétfogú ill. többfogú ligandumok). A ligandumok alkotják az ún. elsö koordinációs szférát, melynek összetétele sztöchiometrikus arányok szerint alakul ki. Oldatok esetén ehhez kapcsolódik a már lényegesen lazább szerkezetü, és sztöchiometrikusan pontosan nem jellemezhetö ún. második koordinációs szféra, amely a van der Waals erök révén lazán kötödö oldószermolekulákból és egyéb oldatkomponensekböl áll.
A kémiában ezen a területen igen fontos az ún. koordinációs szám, amely a központi atom körül maximálisan elhelyezhetö egyfunkciós ligandumok számát jelenti. Ez nagymértékben függ a központi atom vagy ion atom- ill. ionsugarától, annak töltésállapotától azonban független. A koordinációs számok között a 4-es és a 6-os igen gyakori, a 2-es, 5-ös és 8-as koordinációs számok viszont ritkán fordulnak elö. Néhány fémion jellemzö koordinációs száma a17. táblázatban található.
A komplexek elnevezése
A komplexion képletét szögletes zárójelbe tesszük; ha a komplexion pozitív töltésü, a komplexvegyület képletében az elsö, ha negatív töltésü, az utolsó helyen áll ([Ag(NH3)2]Cl és K3[Fe(CN)6]). A komplexion vagy semleges komplexmolekula (Fe(CO)5) képletében a központi fémion vegyjele áll az elsö helyen, melyet a ligandumok követnek a,b,c... sorrendben.
17. táblázat. Fémionok jellemzö koordinációs száma
|
Fémion |
Koordinációs szám |
Példák |
|
Ag+ |
|
[Ag(NH3)2]+ |
|
Ca2+ |
|
[Ca(H2O)6]2+ |
|
Co2+ |
|
[CoCl4]2 , [Co(CN)5]3 , [Co(H2O)6]2+ |
|
Cu2+ |
|
[Cu(NH3)4]2+, [Cu(H2O)6]2+ |
|
Fe2+ |
|
[Fe(CN)6]4 |
|
Pt2+ |
|
[PtCl4]2 |
|
Zn2+ |
|
[Zn(H2O)2 (OH)2] |
|
Co3+ |
|
[Co(NH3)6]3+ |
|
Fe3+ |
|
[FeF6]3 |
Az anion ligandumok neve o-ra végzödik (OH : hidroxo; Cl : kloro; CN :ciano). A semleges- és kation ligandumok neve változatlan marad, kivétel ezek közül az akva (H2O), az ammin (NH3), a karbonil (CO) és a nitrozil (NO) komplexek.
A komplexion vagy csoport nevében a sztöchiometriai arányokat a görög töszámnevekkel jelöljük (mono-, di-, tri-, tetra-, penta-, hexa-); görög sorszámneveket (bisz-, cisz-) használunk akkor, ha a ligandum elnevezésében már van számnév. A központi fémion töltését a név után zárójelbe tett római számmal adjuk meg. Negatív töltésü komplexionok esetében a fémion névhez -át végzödés járul. Fenti elnevezéseket az alábbi példák szemléltetik:
Kelátok
A kelátok olyan komplexek, melyekben a központi atom gyürüt képez a ligandummal. Magától értetödö, hogy ez csak a legalább két funkciós csoporttal rendelkezö ligandum révén lehetséges. Többfogú, vagy legalább két molekula kétfogú ligandum részvételével a központi atom egyidejüleg több gyürüben is szerepelhet.
A kelátok stabilitása általában nagyobb, mint a velük összehasonlítható nem gyürüs komplexeké (keláteffektus). Legnagyobb az öt- és hattagú kelátgyürük stabilitása.
18. táblázat. Fontosabb komplexek elnevezése
|
Elnevezés |
Képlet |
|
kálium-[hexaciano-ferrát(III)] |
K3[Fe(CN)6] |
|
[hexaammin-kobalt(III)]-klorid |
[Co(NH3)6]Cl3 |
|
[tetraammin-dikloro-platina(IV)]-klorid |
[Pt(NH3)4Cl2]Cl2 |
|
vas(0)-pentakarbonil |
[Fe(CO)5] |
|
[trisz(etilén-diamin)kobalt(III)]-klorid |
[Co(en)3]Cl3 |
|
[diciano-argentát(I)]-ion |
[Ag(CN)2] |
A kelát elnevezés egyébként a görög kela (rákolló) szóból ered, utalva ezzel a szóbanforgó komplex molekulaszerkezetére.
Az elözöekre példa, hogy a [Cu(NH3)4]2+-ban a 4 ammóniamolekulát két etilén-diamin molekula is helyettesítheti, amikor is a két etilén-diamin 5 tagú gyürüket alkotva kapcsolódik a réz(II)ionokhoz, a koordinációs szám pedig változatlanul 4 marad. Ez utóbbi komplex rövidített képlete [Cu(en)2]2+ ahol "en" az etilén-diamin ligandumra utal.
A hemoglobin molekulában található hem négyfogú ligandum, míg az etilén-diamin-tetraacetát-ion (EDTA) hatfogú ligandum. A [Fe(EDTA)]2 komplexionban pl. az EDTA négy oxigén és két nitrogénatomon keresztül kapcsolódik a vas(II)ionhoz. A hatfogú ligandum szinte beburkolja a központi fémiont.
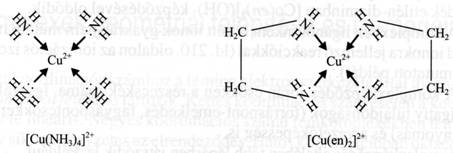
48. ábra Az ammónia molekulák etilén-diaminnal történö helyettesítése
A komplexek képzödése és stabilitása
A fémionok tulajdonságai alapvetöen megváltoznak amikor komplexeket alakítanak ki, mert:
* a komplexképzödés során a legtöbb esetben színváltozás lép fel (a Cu2+ világoskék színü, hidratált ionjának vizes oldatához ammóniát adva sötétkék [Cu(NH3)4]2+ komplexion képzödik),
* a komplexképzödés legtöbbször oldhatóságnövekedéssel jár (a Co(OH)3 csapadék etilén-diaminban [Co(en)3](OH)3 képzödéssel oldódik),
*a komplexben ligandumként kötött ionok nem mutathatók ki a szabad ionokra jellemzö reakciókkal,
*a komplexképzödés során csökken a részecskék száma, így változik a forráspont, a fagyáspont, az ozmózisnyomás (a kolligatív tulajdonságok) és az elektromos vezetöképesség is.
A komplexképzödés mindig több lépésben, lépcsözetesen játszódik le:
![]() Ag+
+ NH3(aq) [Ag(NH3)]+
Ag+
+ NH3(aq) [Ag(NH3)]+
![]() [Ag(NH3)]+ + NH3(aq) [Ag(NH3)2]+
[Ag(NH3)]+ + NH3(aq) [Ag(NH3)2]+
A bruttóegyenlet jelen esetben:
![]() Ag+
+ 2 NH3(aq) [Ag(NH3)2]+
Ag+
+ 2 NH3(aq) [Ag(NH3)2]+
A [diammin-ezüst(I)]-ion képzödésére jellemzö egyensúlyi állandó a komplex stabilitási állandójának (K) felel meg.
K'
=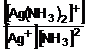 = 1,7
= 1,7
A komplexek stabilitását azok disszociációs állandójának reciprokával, a stabilitási állandóval (K'=1/Kd), vagy ennek logaritmusával (pK) jellemezzük. Az összes többi lépésre felírható egy-egy stabilitási állandó (K1, K2, K3...Ki). Ezek szorzata felel meg a bruttó folyamat stabilitási állandójának (K):
K = K1 · K2 · K3 · Ki
Néhány komplex stabilitási állandóját a 22. táblázat tartalmazza. A táblázatban en-nel az etilén-diamin ligandumot jelöltük.
A stabilitási állandó nagyobb értéke stabilabb komplexre utal. A különbözö fémionok ugyanazzal a ligandummal is eltérö stabilitású komplexeket képezhetnek még azonos koordinációs szám mellett is. Ugyanazzal a ligandummal stabilabb komplex jön létre a fémion oxidációs számának növekedésével. Mint már említésre került, a komplex stabilitását a kelátképzödés fokozza. A ligandum-kicserélödési reakciók lehetösége a stabilitási állandók alapján megjósolható:
![]() [Cd(NH3)4]2+
+ 2 en(aq) [Cd(en)2]2+
+ 4 NH3(aq)
[Cd(NH3)4]2+
+ 2 en(aq) [Cd(en)2]2+
+ 4 NH3(aq)
![]() [Ag(NH3)2]+
+ 2 CN (aq) [Ag(CN)2] + 2 NH3(aq)
[Ag(NH3)2]+
+ 2 CN (aq) [Ag(CN)2] + 2 NH3(aq)
A komplexek geometriai felépítése és izomériája
Az adott koordinációs számhoz a fémion elektronszerkezete által meghatározott geometriai felépítés tartozik. Kettes koordinációs szám esetén a komplex térszerkezete általában lineáris, a négyes koordinációs számú komplexeknél tetraéderes vagy síkban négyzetes, hatos koordinációs számnál oktaéderes, ritkán trigonális prizmás az elrendezödés. Az ötös koordinációs szám viszonylag ritka.
19. táblázat. A komplex ionok stabilitási állandói 25 ° C
|
Komplex ion |
Stabilitási állandó (K) |
|
|
|
[Ag(NH3)2]+ |
|
|
|
[Ag(CN)2] |
|
|
|
[Au(CN)2] |
|
|
|
[Cd(NH3)4]2+ |
|
|
|
[Cd(en)2]2+ |
|
|
|
[Cu(NH3)4]2+ |
|
|
|
[Cu(OH)4]2 |
|
|
|
[Cu(EDTA)]2 |
|
|
|
[Fe(CN)6]4 |
|
|
|
[Fe(CN)6]3 |
|
|
|
[Zn(NH3)4]2+ |
|
|
|
[Zn(EDTA)]2 |
|
|
|
[Co(en)3]2+ |
|
|
|
[Co(en)3]3+ |
|
Biológiailag fontos fémkomplexekben a fehérjemolekulák oldalláncai miatt ezek a szimmetriák torzulnak, mivel sztérikus okok miatt nem tud a geometriailag szabályos elrendezödés kialakulni, valamint azért, mert a ligandumként szereplö kötöhelyek is eltérö eröséggel kapcsolódnak a fémionhoz. A komplexeknek két alapvetö izomériája van: a szerkezeti izomerek a kapcsolódó atomok sorrendjében, a sztereoizomerek pedig a kapcsolódó atomok térbeli elrendezésében különböznek. A szerkezeti izoméria legegyszerübb típusa az ionizációs izoméria, melynek során az azonos tapasztalati képletü komplex vizes oldatában különbözö ionok képzödnek. Példa erre a [Co(NH3)5SO4]Cl és [Co(NH3)5Cl]SO4 komplexek képzödése, melyek közül az elsö vizes oldatából a kloridion kimutatható (ezüstionnal csapadékot ad), de a szulfátion nem ad csapadékot a báriumionnal. A második komplex esetében a kloridion nem mutatható ki, de a szulfátion csapadékot ad a báriumionnal.
A hidrátizoméria is szerkezeti izoméria, melynek során a vízmolekula koordinációs helyzete megváltozik. A különbözö króm(III)ion komplexek színe jellegzetes módon változik meg hidrátizoméria miatt.
[Cr(H2O)6]Cl3 [Cr(H2O)5Cl]Cl2 · H2O [Cr(H2O)4Cl2]Cl · 2 H2O
ibolya világoszöld sötétzöld
Az ibolyaszínü komplexekben a vízmolekulák a Cr elsö koordinációs szférájában ligandumként helyezkednek el, a másik két komplexben egy vagy két vízmolekula már hidrátként, kristályvízként található a második koordinációs szférában. Az ilyen típusú izoméria a vezetöképesség-méréssel is megkülönböztethetö.
A sztereoizoméria alapvetö formája a cisz-transz izoméria, amely a négyes koordinációs számú komplexek diszubsztitúciós származékainál fordul elö.
A hatos koordinációs komplexek egyes típusaira az optikai izoméria a jellemzö, mely az aszimmetrikus szerkezettel függ össze, holott ezek a vegyületek nem tartalmaznak aszimmetriás szénatomot. A két izomer egymásnak fedésbe nem hozható tükörképi párjai. Jellemzö e szerkezetre a [Co(en)3]3+ komplex két enantiomerje.
A komplexeknek igen jelentös szerepe van a különbözö életfolyamatokban igen fontos szerepe van, néhány elem komplexeinek szerepét a 20. táblázat mutatja.
20. táblázat . A fémionok lehetséges szerepe az élö szervezetben
|
Fémion |
Biológiai funkció |
A kapcsolódó ligandum atomja |
A komplex stabilitása |
|
Na+, K+ |
töltésszállítás ingerületátvitel |
O |
kicsi |
|
Ca2+, Mg2+, |
ingerületátvitel, foszfátátvitel, Hidrolízis |
O |
közepes |
|
Mn2+, Zn2+, |
Savkatalízis |
N, S |
nagy |
|
Fe2+/3+, Cu+/2+ |
Redoxikatalízis |
N, S |
nagy |
10. KÉMIAI EGYENSÚLY
Kémiai egyensúlyokról általában
Zárt rendszerben, ahol a molekulák nem hagyhatják el a rendszert, a kémiai reakció elörehaladtával a reagáló anyagok koncentrációi csökkennek, a termékek koncentrációi pedig nönek. Ha egy kémiai reakció A és B molekulák egyesülése C-vé, ennek jelölése reakcióegyenletben:
A + B C
Ha a reakció teljes mértékben lejátszódik, akkor a reakcióközeg kizárólag sztöchiometriai mennyiségü végterméket, C-t tartalmaz. A fenti reakcióban egyensúly is kialakulhat, amikor az egyensúlyi elegyben A, B és C molekula is megtalálható. Az egyensúlyban a koncentrációk állandók, a kémiai folyamatok látszólag leálltak. Az egyensúlyi állapot sokféleképpen jöhet létre. Ha az átalakulatlan, reagáló anyagok koncentrációi nagyobbak, mint a termékeké, akkor a kémiai reakció a reaktánsok irányába van eltolva (legkisebb kényszer elve, ld. késöbb):
![]()
![]() A + B C
A + B C
A termékek irányába eltolt egyensúlyi állapotot az alábbi reakció szemlélteti:
![]() A + B C
A + B C
A kémiai egyensúlyban az elörehaladó és a visszahaladó reakciók azonos sebességgel játszódnak le, így tehát dinamikus egyensúlyi állapotról beszélhetünk. Az egyensúly kialakulása a reakciók sebességével is érzékeltethetö. Pl. foszfor-triklorid (PCl3) és a klórgáz (Cl2) keveréke 500 K körüli hömérsékleten foszfor-pentakloriddá (PCl5) egyesül az elörehaladó reakcióban:
PCl3(g) + Cl2(g) PCl5(g)
Ugyanezen a hömérsékleten a PCl5 bomlása is lejátszódik a visszahaladó reakcióban:
PCl5(g) PCl3(g) + Cl2(g)
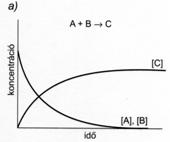
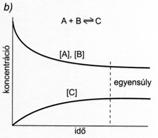
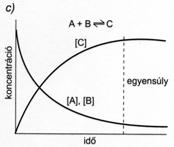
49. ábra. A kémiai egyensúly kialakulása egyirányú, teljes mértékben lejátszódó
(a) és kémiai egyensúlyra vezetö megfordítható (b és c) reakciókban
A B és C = a reaktánsok és a termékek koncentrációja)
A három gáz koncentrációja állandóan változik a keverékben. A kezdeti idöpillanatban az elörehaladó reakció sebessége maximális, majd ez folyamatosan csökken. A visszahaladó reakció sebessége a kezdeti idöpillanatban nulla, mivel még termék nincs jelen, majd a termék koncentrációja növekedésének következtében fokozatosan nö. A gázelegyben mindaddig változik az anyagok koncentrációja ill. az elörehaladó és visszahaladó reakciók sebessége, amíg az egyensúly ki nem alakul. A dinamikus egyensúlyi állapotban az elöre- és visszahaladó reakciók sebessége azonos, ezért az egyensúlyi koncentrációk is állandóak. Idöegység alatt azonos számú kiindulási anyag vagy termékmolekula keletkezik ill. bomlik el.
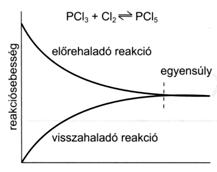
50. ábra. Az elörehaladó és a visszahaladó reakciók sebességének
változása egyensúlyra vezetö folyamatban
Az egyensúlyi állandó
A kémiai egyensúly két ellenkezö irányú folyamat dinamikus egyensúlya. Pl. a nitrogén-dioxid (NO2) átalakulása dinitrogén-tetraoxiddá (N2O4) az alábbi reakcióegyenlettel jellemezhetö egyensúlyra vezet:
![]() 2
NO2(g) N2O4(g)
2
NO2(g) N2O4(g)
Különbözö kezdeti koncentrációjú nitrogén-dioxid gázt használva meghatározható az NO2 és N2O4 egyensúlyi koncentrációja. A kémiai egyensúly jellemzésére az abszolút egyensúlyi koncentrációk helyett, amelyek függnek a kiindulási koncentrációtól, a koncentrációk arányát célszerü használni. A többfajta lehetöség közül akkor kapunk állandó koncentrációarányt, ha a N2O4 NO2 hányadost számoljuk. Ez a hányados kifejezi a kémiai egyensúly sztöchiometriáját is, mivel 1 mol N2O4 képzödéséhez 2 mol NO2 szükséges. A tört értéke független a kiindulási anyagok koncentrációjától, csak a hömérséklettöl függ, ezért egyensúlyi állandónak (K) nevezzük. Ha az egyensúlyban lévö rendszer bármely komponensének koncentrációja megváltozik, a többi komponens koncentrációjának is változni kell, hogy K értéke változatlan maradjon.
Általánosabban megfogalmazva:
![]() aA
+ bB cC + dD,
aA
+ bB cC + dD,
reakcióra vonatkozóan az egyensúlyi állandó definíciószerüen:
K
= ![]() ,
,
ahol [A], [B], [C], [D] a megfelelö anyagok egyensúlyi koncentrációja, míg az a, b, c, d a sztöchiometrikus együtthatók. Az egyensúlyi állandó tehát a keletkezett anyagok megfelelö hatványon szereplö koncentrációjának szorzata, osztva a kiindulási anyagok megfelelö hatványon szereplö koncentrációjának szorzatával. A koncentrációk kitevöi a reagáló anyagok megfelelö együtthatói a reakcióegyenletben. K értéke adott hömérsékleten kísérletileg meghatározható ill. megfelelö termodinamikai adatok ismeretében kiszámítható (DGo -RTlnK). Az egyensúlyi állandó (K) értéke adott hömérsékleten a vizsgált kémiai rendszerre jellemzö termodinamikai (fizikai-kémiai) adat.
Az egyensúlyi állandó fenti definíciója valójában csak a kifejezetten kis koncentrációk esetén érvényes. Ellenkezö esetben a koncentrációk helyett az ún. aktivitásokkal kell számolni. Ez tulajdonképpen az atomok, molekulák és ionok effektív koncentrációja. A tiszta folyékony és tiszta szilárd anyagok egységnyi aktivitásúak. Oldatokban az aktivitást megkapjuk, ha a koncentrációt megszorozzuk az aktivitási koefficienssel. Az aktivitási koefficiens értéke híg oldatokban általában 1, ezért az aktivitás helyett a koncentrációkat is használhatjuk.
Az egyensúlyi állandót számíthatjuk gázfázisban végbemenö reakciókra is, ahol a koncentrációk helyett inkább a parciális nyomással szoktak számolni:
![]() 2
H2(g) + O2(g) 2 H2O(g)
2
H2(g) + O2(g) 2 H2O(g)
K = ![]()
Vizes oldatokban lejátszódó egyensúlyi folyamatra jó példa az ecetsav disszociációja:
![]() CH3COOH(aq)
+ H2O CH3COO + H3O+
CH3COOH(aq)
+ H2O CH3COO + H3O+
K
= ![]()
Egy rosszul oldódó só esetében az egyensúlyra vezetö folyamat az alábbi:
![]() Ag2S(s) 2
Ag+ + S2
Ag2S(s) 2
Ag+ + S2
K = ![]()
Csapadékegyensúlyról lévén szó, adott hömérsékleten Ag2S értéke állandó. Az egyenlet átrendezése után a K Ag2S -t L-nek jelölve:
L = Ag+ S2
ahol L állandó, és a csapadék oldhatósági szorzatát jelenti.
Az egyensúlyi állandók értékei különbözö reakciókra igen eltérök lehetnek, és általában egység nélküli számként adjuk meg azokat. A K számértéke utal az egyensúlyi állapotra is; a K>1 esetén az egyensúly a termékképzödés, K<1 esetén pedig a kiindulási anyagok irányába tolódik el.
A kémiai egyensúly mind a kiindulási irányból, mind a végtermékek felöl elérhetö, pl. a szilárd AgCl oldása a vízben Ag+ és Cl -t eredményez, míg az Ag+ és Cl -ok reakciójából AgCl csapadék keletkezik.
Le Chatelier-elv
Az egyensúlyban lévö kémiai rendszeren mindaddig nem észlelünk változást, amíg a külsö körülmények változatlanok. A külsö körülmények megváltoztatásával új egyensúlyi állapot alakul ki. Ha egy egyensúlyban lévö rendszert külsö hatás ér, akkor a rendszer az egyensúly megváltoztatásával igyekszik a külsö hatást csökkenteni. A koncentrációváltozások, a nyomás- és hömérséklet-változások az elöre- és visszahaladó reakciók sebességét módosítják.
Az ammóniaszintézis példáján a koncentráció és a nyomás megváltoztatásának hatására bekövetkezö folyamatok az alábbiak:
![]() N2(g)
+ 3 H2(g) 2 NH3(g) - ∆H
N2(g)
+ 3 H2(g) 2 NH3(g) - ∆H
Az egyensúly az ammóniaszintézis irányába tolódik el, ha valamelyik kiindulási anyag koncentrációját megnöveljük. A rendszerhez történö N2 hozzáadással fokozódik a szintézis, a hozzáadott nitrogén egy része ammóniává alakul, melynek következtében a külsö hatás csökken. Ammónia hozzáadásával a kiindulási anyagok koncentrációja nö, az egyensúly balra tolódik el. A nyomás növelésével az egyensúly a kevesebb gáz keletkezése, azaz a molekulák számának csökkenése irányába tolódik el. Az ammóniaszintézis példáján bemutatva a nyomás növelése az ammóniaképzödés irányába tolja el az egyensúlyt, mivel 4 mól nitrogén és hidrogén reakciójában csak 2 mól ammónia keletkezik, ezért adott térfogatban, kisebb lesz a nyomás, ami csökkenti a külsö nyomás hatását.
A nyomás megváltoztatása elsösorban a gázfázisú rendszerek egyensúlyát módosítja, és csak csekély befolyást gyakorol a folyékony vagy szilárd anyagokból álló rendszerekre. A hömérséklet hatása gyakorlatilag minden esetben azért jelentös, mert a kémiai egyensúly elöre- és visszahaladó reakciója exoterm (hötermelö), vagy endoterm (höelnyelö) folyamatokból áll. Ha a reakció a termék képzödése irányába exoterm, a kiindulási anyagok irányában endotermnek kell lennie. Ebben az esetben a Le Chatelier-elv értelmében az egyensúlyi rendszer a hömérséklet növelését úgy ellensúlyozza, hogy endoterm (höelnyelö) folyamat játszódik le. Ilyen pl. a higany és az oxigén reakciója:
![]() 2 Hg(l) + O2
(g) 2 HgO(s), DHo
= - 180,7 kJ
2 Hg(l) + O2
(g) 2 HgO(s), DHo
= - 180,7 kJ
A higany-oxid képzödése exoterm folyamat, melyet a DHo negatív elöjele mutat; ezért a hömérséklet növelése az endoterm reakció, vagyis a higanyoxid koncentrációjának csökkenése irányába tolja el az egyensúlyt.
Összefoglalva tehát a kémiai egyensúly változását a külsö hatásokra (Le Chatelier-elv), az alábbiakat lehet elmondani:
*Ha a reaktáns-koncentráció nö vagy a termékkoncentráció csökken, akkor az egyensúly eltolódik a termékképzödés irányába; ha a reaktáns-koncentráció csökken vagy a termékkoncentráció nö, az egyensúly eltolódik a reaktánsképzödés irányába.
*Ha a nyomás növekszik, az egyensúly eltolódik a molekulák számának csökkenése irányába; ha a nyomás csökken az egyensúly eltolódik a molekulák számának növekedése irányába.
Elméleti megfontolások alapján elmondható, hogy az egyensúlyi adott állandó nyomáson a következö egyenlet szerint függ a hömérséklettöl, ahol ∆H a reakcióhö:
d ln K dT RT2 RT2
![]() ∆ H
∆ H
![]()
![]()
![]()
*Hömérséklet növelésével exoterm reakciónál az egyensúly eltolódik a reaktáns képzödés irányába, endoterm reakciónál pedig a termékképzödés irányába; a hömérséklet csökkenésével exoterm reakció esetén az egyensúly a termékképzödés irányába, endoterm reakció esetén pedig a kiindulási anyagok irányába tolódik el.
Elméleti megfontolások alapján elmondható, hogy adott állandó hömérsékleten hogy az egyensúlyi állandó a következö egyenlet szerint függ a nyomástól, ahol ∆V a reakcióelegy reakció utáni végsö és a reakció elötti kezdeti térfogat különbsége:
d ln K dp RT2
![]()
![]() ∆ V
∆ V
![]()
![]()
![]()
Egyensúlyok elektrolitoldatokban
A víz disszociációs egyensúlya, a víz ionszorzata, a pH és a pOH
A tapasztalat szerint még a kémiailag legtisztább víz is vezeti valamennyire az elektromos áramot. Ennek az oka, hogy a víz
![]() H2O + H2O H3O+ + OH
H2O + H2O H3O+ + OH
autoprotolízis (vagy a megszokottabb Arrhenius-féle terminológiát használva disszociáció) révén ionokat is tartalmaz. A folyamat egyensúlyi állandója:
K = ![]() .
.
A víz disszociációjának mértéke nagyon csekély, ezért a disszociálatlan vízmolekulák koncentrációja az öndisszociáció folyamán számottevöen nem változik, összevonható az egyensúlyi állandóval:
K · [H2O]2 = [H3O+] · [OH
A K · [H2O]2 = Kv-t nevezzük a víz ionszorzatának:
Kv = [H3O+] · [OH
Ez az összefüggés minden híg vizes oldatra az oldott anyag anyagi minöségétöl függetlenül igaz. Kv értéke csak a hömérséklettöl függ; 25 oC-on 1,00·10-14.
Kv = [H3O+] · [OH ] = 1,00·10-14 (25 oC-on).
Mivel a víz öndisszociációja azonos koncentrációjú H3O+ és OH ionokat eredményez, ezért a két ion koncentrációja szobahömérsékletü, kémiailag tiszta vízben, valamint a sav- illetve bázisfunkcióra képtelen anyagok (NaCl, K2SO4 stb.) vizes oldataiban egyenlö:
[H3O+] = [OH 1,00·10-7 mol/dm3.
Az olyan vizes oldatokat, amelyekben az oxónium és a hidroxidionok koncentrációja is 1· 10-7 mol/dm3, semleges vagy neutrális oldatoknak nevezzük. Savas oldatokban az oxóniumion-koncentráció nagyobb, mint 1· 10-7 mol/dm3, míg lúgos (bázikus) oldatokban kisebb ennél. A víz ionszorzatát alkalmazhatjuk savak vagy bázisok vizes oldataira is. Sav bevitele megnöveli az oxóniumion-koncentrációt, ezért az egyensúly a H2O képzödése irányába tolódik el, csökkentve ezzel a hidroxidionok koncentrációját. Lúg bevitelével a hidroxidionok koncentrációja növekszik, míg a hidroxóniumionok koncentrációja csökken a disszociációs egyensúlyi állandó változatlanul maradása mellett.
A vízben lévö hidroxid- és oxónium ionok koncentrációjával kapcsolatban fennáll az a kényelmetlenség, hogy túl kis számokkal (a 10 negatív kitevöjü hatványaival) vagyunk kénytelenek számolni. Az ezekkel kapcsolatos függvények ábrázolása is némi nehézséget okozhat, mivel a szóbanforgó ionok koncentrációtartománya több nagyságrendet ölel fel. Ezek figyelembevételével tisztán praktikus meggondolás alapján került bevezetésre a pH- és a pOH-fogalom, melyek definíciója híg oldatok esetén ( lg tízes alapú logaritmust jelent ):
pH = - lg [H3O+]
pOH = - lg [OH
Tehát a pH a hidroxóniumion-koncentráció negatív logaritmusa, a pOH pedig a hidroxidion-koncentráció negatív logaritmusa.
Fentiek szerint semleges kémhatású vizes közeg esetén:
pH = pOH = 7,
savas és lúgos oldatok esetén pedig:
pH< 7 ill. pH >
A pH és pOH mellett bevezethetjük a pKv = -lgKv, melynek segítségével a víz ionszorzata (Kv = [H3O+] · [OH ] = 1,00·10-14; 25 oC-on) helyett a következöt is felírhatjuk:
pH + pOH = pKv
25 oC-on pKv = 14.
A pH jelentése hidrogénkitevö, amely a hatványkitevöre utal, ennek megfelelöen a hidroxóniumion-koncentráció 10-szeres változása 1 pH egységnek felel meg. Különbözö oldatok pH és pOH értékeit a 24. táblázat tartalmazza.
Gyenge savak disszociációs egyensúlya
Egy HA általános képletü sav vizes oldatban lejátszódó protolitikus reakciója a következö:
![]() HA + H2O H3O+ + A
HA + H2O H3O+ + A
A sav disszociációjának egyensúlyi állandója az alábbi:
K's
= ![]()
mely kifejezés egyszerüsíthetö, mivel a víz koncentrációja gyakorlatilag állandó, mely így összevonható a K's állandóval:
![]()
A Ks a sav disszociációs egyensúlyi állandója. A sav annál erösebb, minél nagyobb a Ks értéke. Erös savak gyakorlatilag teljes mértékben disszociálnak, ezért az erös savak (HCl, HNO3, H2SO4 elsö disszociációs lépése) Ks értékei a 25. táblázatban nem találhatók.
A középerös és
gyenge savak Ks ill. pKs értékeit csökkenö savi
erösség sorrendjében a 24. táblázat tartalmazza. A táblázatban található
néhány többértékü sav protolitikus reakciója is. Látható például, hogy a
foszforsav középerös savnak tekinthetö az elsö proton
disszociációja alapján, míg nagyon gyengének a harmadik proton disszociációja
szerint. Gyenge savakban a disszociáció csak kismértékü (disszociáció% = ![]() ·100), értékét az
egyensúlyi hidroxóniumion-koncentrációból és az összes savkoncentrációból
számíthatjuk.
·100), értékét az
egyensúlyi hidroxóniumion-koncentrációból és az összes savkoncentrációból
számíthatjuk.
A disszociáció foka változik a sav koncentrációjával; gyenge savak esetében hígítással a disszociáció foka növelhetö. A növekvö disszociáció összhangban van a Le Chatelier-elvvel: a növekvö hígítás, víz hozzáadása, az egyensúlyt jobbra tolja el:
![]() CH3COOH(aq)
+ H2O(l) CH3COO + H3O+
CH3COOH(aq)
+ H2O(l) CH3COO + H3O+
21. táblázat. Savas, semleges és lúgos vizes oldatok
pH és pOH értékei 25 oC-on
|
[H+] mol/dm3 |
pH |
pOH |
[OH ] mol/dm3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Savas 12 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
semleges 7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Lúgos 3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
22. táblázat. Savak disszociációs egyensúlya; Ks és pKs értékei 25 oC-on
Sav Disszociációs egyensúly Ks pKs
![]() Foszforsav (1.) H3PO4 H+ + H2PO
Foszforsav (1.) H3PO4 H+ + H2PO![]() 7,5· 10-3 2,12
7,5· 10-3 2,12
![]() Hidrogén-fluorid HF H+ + F 6,5·10-4 3,19
Hidrogén-fluorid HF H+ + F 6,5·10-4 3,19
![]() Ecetsav CH3COOH H+ + CH3COO 1,8· 10-5 4,74
Ecetsav CH3COOH H+ + CH3COO 1,8· 10-5 4,74
![]() Szénsav (1.) H2CO3 H+ + HCO
Szénsav (1.) H2CO3 H+ + HCO![]() 4,5· 10-7 6,35
4,5· 10-7 6,35
![]() Foszforsav (2.) H2PO
Foszforsav (2.) H2PO![]() H+ + HPO
H+ + HPO![]() 6,2·
10-8 7,21
6,2·
10-8 7,21
![]() Ammóniumion NH
Ammóniumion NH![]() H+
+ NH3 6,3·
10-10 9,20
H+
+ NH3 6,3·
10-10 9,20
![]() Hidrogén-cianid
HCN H+
+ CN 6,2· 10-10 9,21
Hidrogén-cianid
HCN H+
+ CN 6,2· 10-10 9,21
![]() Szénsav (2.) HCO
Szénsav (2.) HCO![]() H+
+ CO
H+
+ CO![]() 5,6· 10-11 10,25
5,6· 10-11 10,25
![]() Foszforsav (3.) HPO
Foszforsav (3.) HPO![]() H+ + PO
H+ + PO![]() 4,8·
10-13 12,32
4,8·
10-13 12,32
Gyenge savaknál az oldat pH értéke nem számítható az erös savaknál alkalmazott módon. A számításhoz a koncentráción kívül a disszociációs egyensúlyi állandó (Ks) értékét is fel kell használni.
A pH-hoz hasonlóan esetenként megkönnyíti a számolást, ha a disszociációs egyensúlyi állandó helyett annak negatív logaritmusával, a pKs-sel dolgozunk. A savkitevö vagy savexponens definíciója:
pKs = - lgKs
Gyenge bázisok disszociációs egyensúlya
Egy BOH gyenge bázis vizes oldatában az alábbi egyensúly áll fenn:
![]() B
+ H2O HB+
+ OH
B
+ H2O HB+
+ OH
A bázis disszociációjának egyensúlyi állandója:
![]() .
.
A víz koncentrációja gyakorlatilag állandó, ezért összevonható a Kb' egyensúlyi állandóval:
Kb
= Kb'· H2O = ![]() .
.
A pKs-hez hasonlóan definiálhatjuk a pKb-t, a báziskitevöt vagy bázisexponenst. Ennek definíciója:
pKb = - lgKb.
A közepes erösségü és igen gyenge bázisok Kb és pKb értékeit a csökkenö báziserösség sorrendjében a 23. táblázat tartalmazza.
23. táblázat. A bázisok disszociációs egyensúlyi reakciói; Kb ill. pKb értékei
Bázis Disszociációs egyensúly Kb pKb
![]() Karbonátion CO
Karbonátion CO![]() + H2O HCO
+ H2O HCO![]() + OH 2,1·10-4 3,68
+ OH 2,1·10-4 3,68
![]() Trimetil-amin (CH3)3N + H2O (CH3)3N+H
+ OH 6,2·10-5 4,20
Trimetil-amin (CH3)3N + H2O (CH3)3N+H
+ OH 6,2·10-5 4,20
![]() Ammónia NH3 + H2O NH
Ammónia NH3 + H2O NH![]()
![]() + OH 1,6·10-5 4,80
+ OH 1,6·10-5 4,80
![]() Acetátion CH3COO +
H2O CH3COOH
+ OH 5,6·10-10 9,26
Acetátion CH3COO +
H2O CH3COOH
+ OH 5,6·10-10 9,26
![]() Fluoridion F +
H2O HF + OH 1,5·10-11 10,81
Fluoridion F +
H2O HF + OH 1,5·10-11 10,81
A bázis erössége annál nagyobb, minél nagyobb a Kb. Gyenge savak anionjai viszonylag erös bázisnak, erösebb savak anionjai pedig viszonylag gyenge bázisnak tekinthetök.
Ks és a Kb összefüggése konjugált sav és bázis esetén
A korábban bevezetett jelöléseket alkalmazva:
![]() HA + H2O H3O+ + A
HA + H2O H3O+ + A
Ennek megfelelöen a K's:
K's
= ![]() .
.
Ugyanakkor:
![]() A + H2O HA
+ OH
A + H2O HA
+ OH
Aminek megfelelöen:
K'b
= ![]()
Fentiek alapján:
K's
K'b = ![]()
A nevezövel beszorozva:
K's K'b H2O = H3O+ OH- = Kd(víz) H2O
tehát:
Ks · Kb = Kv.
A hidrogén-fluorid példáján az összefüggés az alábbiak szerint mutatható be:
![]() HF(aq) H+ + F
HF(aq) H+ + F
Ks
= ![]() .
.
A konjugált bázis és a fluoridion disszociációs egyensúlya az alábbi:
![]() F + H2O(l) HF(aq) + OH
F + H2O(l) HF(aq) + OH
Kb = ![]()
Ks
Kb =![]() = H+ OH = Kv
= H+ OH = Kv
Ionok reakciója vízzel
Az ionok vizes oldataikban hidrátburokkal vannak körülvéve, ezért az ionokat az alábbiak szerint is írhatjuk:
![]() K+ + mH2O(l) [K(H2O)m]+
K+ + mH2O(l) [K(H2O)m]+
![]() Cl + nH2O(l)
[Cl(H2O)n]
Cl + nH2O(l)
[Cl(H2O)n]
Az ionok esetenként nemcsak hidratálódnak, hanem megváltoztatják a víz disszociációs egyensúlyát is, savas vagy lúgos oldatokat létrehozva.
A poláris vízmolekula az erös bázisok kationjait olyan hidrátburokkal veszi körül, mely viszonylag lazán kötött. Az erös savakban található anionok is hidratálódnak; mint minden bázis potenciális protonakceptoroknak tekinthetök, de nem képesek protonfelvételre a vízmolekulától. Vannak azonban olyan kationok és anionok is, melyek reagálnak a vízzel. A vízzel reagáló kationok közé tartoznak pl. a nitrogén tartalmú kationok és a nagy polarizációs képességü fémionok, melyek kisméretüek és többszörös pozitív töltésüek. Az ammóniumion és a víz reakciója a protolitikus folyamatokban az alábbi:
![]() NH
NH![]() + H2O(l) NH3 + H3O+,
+ H2O(l) NH3 + H3O+,
sav1 bázis2 bázis1 sav2
melyben H3O+ képzödik a Brönsted-Lowry-elmélet alapján; az oldat kémhatása ezért savas. Bizonyos fémionok vízzel történö reakciója is savas oldatot eredményezhet:
![]() Al3+ + 2 H2O(l ) Al(OH)2++ H3O+
Al3+ + 2 H2O(l ) Al(OH)2++ H3O+
A fémionok protolitikus folyamatának mechanizmusa azonban ennél bonyolultabb. A hidratált fémion reagál a vízzel:
![]() [Al(H2O)6]3+
+ H2O(l) Al(H2O)5(OH)]2+
+ H3O+,
[Al(H2O)6]3+
+ H2O(l) Al(H2O)5(OH)]2+
+ H3O+,
sav1 bázis2 bázis1 sav2
így a hidrátburok egyik kötött vízmolekulájának protonja adódik át valamelyik szabad vízmolekulának.
A gyenge savakban található anionok hidratálódnak is, és a vízzel is reagálnak. A víz protonjaival reagálva gyenge savak jönnek létre, és a felszaporodó hidroxidionok miatt az oldat kémhatása lúgos lesz. A lejátszódó protolitikus reakció az alábbi:
![]() CH3COO + H2O(l)
CH3COOH + OH
CH3COO + H2O(l)
CH3COOH + OH
![]() S2- + H2O(l) HS + OH
S2- + H2O(l) HS + OH
bázis1 sav2 sav1 bázis2
Az ionok vízzel történö reakciójáról és a vizes sóoldatok kémhatásáról az alábbi összeállítás ad információt:
Vizes sóoldatok kémhatása: a hidrolízis
Az elözö táblázat alapján a vizes sóoldatok 4 típusba sorolhatók:
* Semleges kémhatású sóoldatok: az oldódás során sem az anion sem a kation nem reagál a vízzel, hanem hidratálódik. Ilyenek pl. az alkálifémek kloridjai, klorátjai és nitrátjai.
*Lúgos kémhatású sóoldatok: az oldódás során csak az anion reagál a vízzel, ilyenek pl. az alkálifémek, a Ca2+ és a Ba2+ karbonátjai, foszfátjai és acetátjai.
*Savas kémhatású sóoldatok: az oldódás során csak a kation reagál a vízzel; a d mezö kationjai és az ammóniumion alkotnak ilyen típusú sókat nitráttal, kloriddal és bromiddal.
*Változó kémhatású sóoldatok: a kation és az anion is reagál a vízzel, melynek során a két vízzel reagáló ion reakciójának mértéke határozza meg az oldat pH-ját. Ilyen pl. az ammónium-acetát vizes oldata.
24. táblázat Ionok reakciója vízzel és a vizes sóoldatok kémhatása

KATIONOK
![]() hidratálódnak hidratálódnak és
hidratálódnak hidratálódnak és
vízzel reagálnak
Li+, Na+, K+, NH![]() , Zn2+, Al3+,
, Zn2+, Al3+,
Ca2+, Ba2+ Fe3+, Cr3+, Cu2+

hidratálódnak semleges kémhatás savas kémhatás
NO![]() , Cl , Br NaCl, CaCl2, KNO3 NH4Cl, AlCl3,
, Cl , Br NaCl, CaCl2, KNO3 NH4Cl, AlCl3,
|
|
I , ClO![]() , ClO
, ClO![]() Fe(NO3)3
Fe(NO3)3
hidratálódnak és lúgos kémhatás változó pH (gyengén
vízzel reagálnak savas vagy lúgos)
PO![]() , CO
, CO![]() , S2- Ba(CH3COO)2, NH4(CH3COO),
, S2- Ba(CH3COO)2, NH4(CH3COO),
CN , SO![]() , HCO
, HCO![]() K2CO3,
Na2S, NH4NO2,
K2CO3,
Na2S, NH4NO2,
CH3COO , NO![]() , F KCN NH4CN
, F KCN NH4CN
A kationok és anionok reakcióját a vízzel hidrolízisnek hívjuk, mely valójában egy sav-bázis reakció. A Brönsted-Lowry-elmélet szerint az anion (A-) reakciója a vízzel konjugált sav (HA) és hidroxidion keletkezéssel jár:
![]() A + H2O(l)
HA(aq) + OH
A + H2O(l)
HA(aq) + OH
Az egyensúlyi állandó kifejezése a fenti folyamatra az alábbi:
Kb
= ![]()
Nátrium-acetát esetében a vizes oldatban anion hidrolízis játszódik le, melyre alkalmazva a fenti általános összefüggést, az alábbiakat kapjuk:
![]() CH3COO + H2O(l) CH3COOH(aq) + OH
CH3COO + H2O(l) CH3COOH(aq) + OH
Kb = ![]() ,
,
ahol Kb az acetátionra jellemzö disszociációállandó.
Táblázatból az ecetsav disszociációállandó értékét kikeresve, a Kb értéke a víz ionszorzata segítségével kiszámítható:
Kb
= ![]() .
.
Az ammónium-klorid vizes oldatában kation hidrolízis játszódik le, melynek során az ammóniumion reagál a vízzel, konjugált bázist (NH3) és oxóniumiont hozva létre:
![]() NH
NH![]() + H2O(l) NH3(aq) + H3O+.
+ H2O(l) NH3(aq) + H3O+.
A reakció alapján felírható a disszociációs egyensúlyi állandó:
Ks
= ![]() .
.
A kation és anion hidrolízisekor két
egyensúly alakul ki, melyek Ks és Kb disszociációs
állandókkal jellemezhetök. Ha Ks > Kb, akkor az
oldat savas, ha Ks < Kb, akkor az oldat lúgos
kémhatású lesz. Az ammónium-nitrit vizes oldatában pl. Ks = 6,3·10-10
az ammóniumionra és Kb = 1,4·10-
A közös ion hatása
Ha az egyensúlyi rendszerhez a reakció termékét adjuk hozzá, az egyensúly a kiindulási anyagok irányába tolódik el. Mg(OH)2 telített oldatához NaOH-t adva a közös OH ion megváltoztatja az egyensúlyi állapotot.
![]() Mg(OH)2(s) Mg2+ + 2 OH
Mg(OH)2(s) Mg2+ + 2 OH
![]() közös
ion
közös
ion
A hidroxidionok reagálnak a Mg2+ ionokkal, és Mg(OH)2 csapadék válik ki. A közös ion hozzáadásával módosítani lehet gyenge savak vagy gyenge bázisok disszociációs egyensúlyát és így pH-értékét is. Gyenge sav oldatához erös savat adva az visszaszorítja a gyenge sav disszociációját, mivel a H3O+ ionok mindkét sav disszociációjának közös termékei. Az ecetsav disszociációja visszaszorítható nátrium-acetáttal is.
Sav-bázis indikátorok
A sav-bázis indikátorok olyan gyenge savak vagy gyenge bázisok, amelyek konjugált ionjai más színüek, mint a semleges molekula. Az acidi-alkalimetriás indikátorok gyengén savanyú vagy gyengén bázikus karakterü festékek, amelyek savanyú közegben más színt mutatnak mint lúgos közegben, amely rendszerint a molekula belsö átrendezödésének következménye.
Az indikátorok jellemzésére kettö adat szolgál:
*az indikátor átcsapási pontja vagy indikátorexponense, és az
*az indikátor átcsapási tartománya.
Az indikátor átcsapási pontja (indikátorexponens) az a pH, amelynél az indikátor savanyú és lúgos alakja egyenlö koncentrációban van jelen.
Hind disszociációjára vizes oldatban a következö egyenlet írható fel:
![]() Hind + H2O Ind + H3O+.
Hind + H2O Ind + H3O+.
A reakcióra felírható a tömeghatás törvénye:
![]() .
.
Nagy hidrogénion-koncentrációnál az oldat színét a Hind színe határozza meg. Ha a hidrogénion koncentráció kicsi (lúgos környezet), a konjugált bázis (Ind-) színe szabja meg az oldat színét. Az elöbbi egyenletet átrendezve és mindkét oldal negatív logaritmusát véve a következö összefüggéshez jutunk:
pH =
![]() .
.
Az átcsapási pontban a disszociált és a disszociálatlan indikátor koncentrációja egymással megegyezik, azaz [Hind] = [Ind ], azaz pH = pKind, vagyis az átcsapási pont pH-ja savanyú indikátorok esetében megegyezik az egyensúlyi állandó negatív logaritmusával, melyet indikátorexponensnek nevezünk.
Az indikátor színátcsapásának pH-tartományát annak disszociációállandója határozza meg. A szem érzékenysége a színváltozásokra eléggé korlátozott, ezért az egyik szín mellett a másikat csak akkor veszi észre, ha ez a másiknak legalább 10 %-át kiteszi. Átcsapást tehát a koncentrációviszonyok 100-szoros változása fogja jelenteni, ezért a szín változása kb. 2 pH egységen belül történik meg. A sav-bázis titrálásnál az az ideális, ha már 1 csepp titrálóoldat hatására végbemegy a színváltozás, azaz az indikátor különbözö formái koncentrációviszonyának 100-szoros megváltozása, ezért célszerü a titrálást igen kis mennyiségü indikátor jelenlétében végezni. Azok a jó indikátorok, amelyeknél legalább az egyik forma igen intenzív színü, ahol a színátcsapás könnyen megfigyelhetö. Néhány indikátor színátcsapási pH-tartományát a 28. táblázat tartalmazza:
25. táblázat. Sav-bázis indikátorok színváltozása
|
Indikátor |
Egyik szín (kisebb pH-nál) |
pH tartomány |
Másik szín (nagyobb pH-nál) |
|
Metilnarancs |
Vörös |
|
sárga |
|
Fenolftalein |
Színtelen |
|
vörös |
Pufferoldatok
Pufferoldatoknak nevezzük a gyenge savat és a gyenge savaknak erös bázisokkal alkotott sóját, vagy gyenge bázist és gyenge bázisnak erös savval alkotott sóját tartalmazó oldatokat. A puffer oldat pH-ja csak kismértékben változik meg akkor, ha erös savat vagy erös bázist adunk hozzá.
Pufferoldatok pH kiegyenlitö hatásának értelmezése konkrét esetben. Savas puffer rendszer az ecetsav és a nátrium-acetát rendszer, illetve lúgos az ammónium -hidroxid ammónium-klorid rendszer.
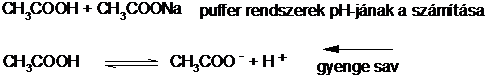
[CH3COO-]
.[ H+] Ks = [ CH3COOH
]
![]()
![]()
egyensúlyok alapján : sav = gyenge sav [ mol/dm3]
c sav - [H+] ≈ [CH3COOH] = sav
[CH3COO-] = [CH3COONa]
c só - [H+] ≈ [ CH3COONa]= só
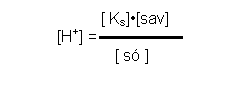
Henderson Hasselbach egyenlet
- lg [ H+ ] = - lg Ks + lg [ só ]/[sav ]
pH = pKs + lg [ só ]/[sav ]
pH értéke függ :
* Ks, a gyenge sav anyagi minösége,
* sav/ só koncentráció aránytól
Pufferoldatok kiegyenlitö hatásának mechanizmusa:
* erös sav hozzáadása a rendszerhez, "a" mol HCl esetében
![]() CH3COO- + H+
+ Cl- CH3COOH
+ Cl-
CH3COO- + H+
+ Cl- CH3COOH
+ Cl-
-"a" + "a" + "a"
[ c sav + "a"]
 [ H+ ] = Ks .
[ H+ ] = Ks .
[ c só - "a" ]
* erös bázis hozzáadása esetében, "b" mol NaOH esetében
CH3COOH + NaOH = CH3COONa + H2O
- "b" + "b" + "b"
[ c sav -"b"]
 [ H+ ] = Ks .
[ H+ ] = Ks .
[ c só + "b"]
A hozzáadott "a" illetve "b" mól mennyisége igen csekély, ezért egy adott intervallumon belül nem változik sav/só koncentráció aránya, így pH értéke sem, mivel azt a Ks , az illetö gyenge sav anyagi minösége határozza meg.
NH4OH/NH4Cl puffer rendszer pH-jának a számítása
![]()
[NH4+].[OH-]
Kb
= ![]()
[NH4OH]
![]()
[NH4OH] = cgyenge bázis - OH- ≈ c bázis
[NH4+] = c só + NH4+ ≈ c só
[c só].[OH-]
Kb
= ![]()
[c bázis]
[ Kb].[bázis]
![]() [OH-] =
[OH-] =
[ só ]
Henderson Hasselbach egyenlet
- lg [OH-] = - lg Kb + lg [ só ]/[bázis ]
pOH = pKb + lg [ só ]/[bázis ]
* erös bázis hozzáadása a rendszerhez, "c" mol NaOH esetében
![]() OH- + NH4+ NH4+
OH- + NH4+ NH4+
+ "c" - "c" - "c "
[ Kb ].[bázis + c]
![]() [OH-] =
[OH-] =
[ só - c ]
* erös sav hozzáadása a rendszerhez, "d" mol HCl esetében
NH4OH + HCl = NH4Cl
- "d" + "d" + "d"
[ Kb ].[bázis -d]
![]() [OH-] =
[OH-] =
[ só + d]
A hozzáadott "a" illetve "b" mól mennyisége igen csekély, ezért egy adott intervallumon belül nem változik bázis/só koncentráció aránya, így pH értéke sem, mivel azt a Kb , az illetö gyenge bázisanyagi minösége határozza meg.
A pufferoldatok jellemzöje a puffertartomány, vagyis az a pH-határérték, amely között a puffer hatásosan müködik. A célnak megfelelö puffertartományú pufferoldat készítéséhez olyan savat vagy bázist kell felhasználni, amelynek pKs ill. pKb értéke közel van a kívánt pH-hoz. Az [sav[/[só] illetve [bázis]/[só] arányt úgy célszerü megválasztani, hogy az 0,1-10 közzé essen, mert így a puffertartomány gyakorlatilag két pH-egység.
A pufferkapacitás valamely erös bázisnak ill. erös savnak mol/dm3-ben kifejezett azon mennyisége, amely az adott pufferrendszer pH-ját egy egységgel változtatja meg. A pufferkapacitást a protonakceptor és a protondonor koncentrációja, valamint azok aránya határozza meg. Minél nagyobb a sav vagy a só koncentrációja, annál több erös bázis vagy erös sav hozzáadása szükséges a puffer pH-jának lényeges megváltoztatásához.
Az elektrolitok oldhatósága és az oldhatósági szorzat
Az elektrolitok oldhatósága alatt a telített oldat koncentrációját értjük egy adott hömérsékleten. Az oldhatóság mértékegysége a g/dm3, vagy a mol/dm3. Az utóbbi esetben a moláris oldhatóságról beszélünk.
Telített vizes oldatokban dinamikus egyensúlyi állapot jön létre, amikor az oldat koncentrációja már nem növelhetö, tehát idöegység alatt ugyanannyi anyag oldódik fel, mint amennyi kiválik. Ionkristályok oldása esetén az oldatban ionok találhatók. Ha ezüst-klorid csapadék desztillált vízzel érintkezik, az alábbi egyensúly alakul ki:
![]() AgCl(s) Ag+ + Cl
AgCl(s) Ag+ + Cl
A fenti egyensúly alakul ki akkor is, ha ezüst-nitrát oldatot elegyítünk nátrium-klorid oldattal, de a folyamat most a termékek irányából indul el; a kémiai egyensúly tehát mindkét oldalról elérhetö. A reakció lejátszódásának mértékét mindkét esetben az ezüst-klorid oldhatósága határozza meg. A folyamatra felírható az alábbi egyensúlyi állandó:
K
= ![]() .
.
Mivel a szilárd AgCl koncentrációja állandó, ez összevonható a K-val:
L = K · [AgCl] = [Ag+ ·[Cl
ahol L = oldhatósági szorzat.
Ez a módosított egyensúlyi állandó a nehezen oldódó ionkristályos anyagok oldódási irányba felírt folyamatára vonatkozik. Néhány só oldhatósági szorzatát 25 oC-on a 26. táblázat tartalmazza.
26. táblázat. Oldhatósági szorzatok 25 oC-on
|
Vegyület |
L |
Vegyület |
L |
|
AgCl |
|
CaCO3 |
|
|
Ag2CrO4 |
|
Ca3(PO4)2 |
|
|
AgBr |
|
FeS |
|
|
AgI |
|
Fe(OH)3 |
|
|
Al(OH)3 |
|
Hg2Cl2 |
|
|
BaSO4 |
|
PbCl2 |
|
|
CaSO4 |
|
PbSO4 |
|
Az oldhatóság és az oldhatósági szorzat szorosan összefüggö, de nem azonos fogalmak. A moláris oldhatóság a telített oldatban az ionok egyensúlyi koncentrációjával azonos bizonyos hömérsékleten. Az alábbiakban az oldhatóság és az oldhatósági szorzat közötti eltérés kerül bemutatásra a bárium-szulfát és az alumínium-hidroxid segítségével. A bárium-szulfát esetében az oldódás a következök szerint megy végbe:
![]() BaSO4(s) Ba2+ + SO
BaSO4(s) Ba2+ + SO![]() .
.
x x
Ebben az esetben a [Ba2+]
= [SO![]() ] = x, vagyis az
ionkoncentrációk azonosak a moláris oldhatósággal.
] = x, vagyis az
ionkoncentrációk azonosak a moláris oldhatósággal.
A BaSO4 esetében az oldhatósági szorzat:
L
= [Ba2+]·[SO![]() ] = x·x = x2.
] = x·x = x2.
Ebböl látható, hogy különbözö anyagoknál igen eltérö oldhatósági szorzatok hasonló oldhatóságokat, és a hasonló oldhatóságok igen eltérö oldhatósági szorzatokat eredményezhetnek.
Az oldhatósági szorzat ismeretében az oldatban lévö ionkeverékek szétválasztása megfelelöen megválasztott kicsapó szerekkel elvégezhetö. Szelektíven kicsapatva a legkevésbé oldódó anyagot, az a rendszerböl szüréssel eltávolítható, majd a kicsapás folytatható a következö reagenssel. A reagenseket úgy kell megválasztani, hogy a csapadékok oldhatósága között nagy legyen a különbség. Az oldhatóságot jelentösen csökkenti a közös ion.
![]() Ha pl. ezüst-szulfát
(Ag2SO4) csapadékkal érintkezö telített oldathoz
ezüst-nitrátot (AgNO3) vagy nátrium-szulfátot (Na2SO4)
adunk, az oldódási egyensúly megbomlik, és hogy az ismét beálljon, további csapadékképzödés
történik, vagyis mindkét esetben csökken az ezüst-szulfát oldhatósága. Ennek
természetesen az ellenkezöje megy végbe akkor, ha a telített oldatot
vízzel hígítjuk. Mind a közös ion hozzáadásakor, mind a vízzel való hígítás
esetén a legkisebb kényszer elve érvényesül. Ag2SO4(s) 2 Ag2+ + SO
Ha pl. ezüst-szulfát
(Ag2SO4) csapadékkal érintkezö telített oldathoz
ezüst-nitrátot (AgNO3) vagy nátrium-szulfátot (Na2SO4)
adunk, az oldódási egyensúly megbomlik, és hogy az ismét beálljon, további csapadékképzödés
történik, vagyis mindkét esetben csökken az ezüst-szulfát oldhatósága. Ennek
természetesen az ellenkezöje megy végbe akkor, ha a telített oldatot
vízzel hígítjuk. Mind a közös ion hozzáadásakor, mind a vízzel való hígítás
esetén a legkisebb kényszer elve érvényesül. Ag2SO4(s) 2 Ag2+ + SO![]()
![]() közös ion
közös ion
Találat: 17571